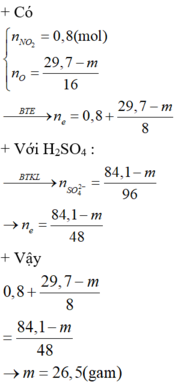Bài 31. Cho 7,6 gam hỗn hợp gồm Fe, Mg, Cu vào dung dịch H2SO4 đặc, nguội dư thì thu được 6,16 lit khí SO2 (đktc). Phần không tan cho tác dụng với dd HCl dư thu được 1,12 lit khí (đkc). Tính % khối lượng hỗn hợp đầu.

Những câu hỏi liên quan
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau
- Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2
- phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G
- phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu...
Đọc tiếp
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau - Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2 - phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G - phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu được b gam chất rắn E biết các phản ứng xảy ra hoàn toàn. Tính giá trị của a và b Làm hộ em với ạ!!!。゚( ゚^∀^゚)゚。
Cho 10,38 gam hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lit khi (đktc).Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lit khí SO2 (đktc).a. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.b. Tính số mol axit tham gia phản ứng ở mỗi phần.
Đọc tiếp
Cho 10,38 gam hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:
Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lit khi (đktc).
Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lit khí SO2 (đktc).
a. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.
b. Tính số mol axit tham gia phản ứng ở mỗi phần.
a)
Gọi số mol Fe, Al, Ag trong mỗi phần là a, b,c (mol)
=> 56a + 27b + 108c = 5,19 (1)
Phần 1:
\(n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----->a------------------>a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b------>1,5b------------------->1,5b
=> a + 1,5b = 0,105 (2)
Phần 2:
\(n_{SO_2}=\dfrac{2,912}{22,4}=0,13\left(mol\right)\)
PTHH: 2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
b----->3b-------------------->1,5b
2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------>3a--------------------->1,5a
2Ag + 2H2SO4 --> Ag2SO4 + SO2 + 2H2O
c-------->c------------------>0,5c
=> 1,5a + 1,5b + 0,5c = 0,13 (3)
(1)(2)(3) => a = 0,03 (mol); b = 0,05 (mol); c = 0,02 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=2.0,03.56=3,36\left(g\right)\\m_{Al}=2.0,05.27=2,7\left(g\right)\\m_{Ag}=2.0,02.108=4,32\left(g\right)\end{matrix}\right.\)
b)
- Phần 1:
\(n_{H_2SO_4}=a+1,5b=0,105\left(mol\right)\)
- Phần 2:
\(n_{H_2SO_4}=3a+3b+c=0,26\left(mol\right)\)
Đúng 3
Bình luận (0)
Cho 18,2 gam hỗn hợp các kim loại Fe, Cr, Cu tác dụng với lượng dư dung dịch
H
2
SO
4
loãng, nóng trong điều kiện không có không khí thu được dd Y và chất rắn Z cùng 5,6 lít
H
2
(đktc). Nếu cho 18,2 gam X tác dụng với lượng dư dd
H
2
SO
4
đặc, nguội thu được 1,68 lít khí
SO
2...
Đọc tiếp
Cho 18,2 gam hỗn hợp các kim loại Fe, Cr, Cu tác dụng với lượng dư dung dịch H 2 SO 4 loãng, nóng trong điều kiện không có không khí thu được dd Y và chất rắn Z cùng 5,6 lít H 2 (đktc). Nếu cho 18,2 gam X tác dụng với lượng dư dd H 2 SO 4 đặc, nguội thu được 1,68 lít khí SO 2 (đktc). Tính thành phần phần trăm crom trong hỗn hợp?
A. 42,86%
B. 52%
C. 26,37%
D. 43%.
Chia 35 8 gam hỗn hợp x gồm Al, Fe, Cu thành 2 phần bằng nhau: Phần 1: cho tác dụng với dung dịch H2SO4 đặc nguội thì thu được 3,36 lít khí SO2 (ở đktc) Phần 2: cho tác dụng với dung dĩhj H2SO4 loãng thấy thoát ra 5,6 lít khí H2 (ở đktc) Tính khối lượng kim loại trong X. Mong mn trả giúp e sớm tại e sắp thi giữa kỳ r =((
\(\text{Mỗi phần,gọi :} n_{Al} = a ; n_{Fe} = b ; n_{Cu} = c\\ \Rightarrow 27a + 56b + 64c = \dfrac{35,8}{2} = 17,9(1)\\ \text{Phần 1 : Al,Fe không phản ứng với axit đặc nguội}\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O\\ n_{Cu} = c = n_{SO_2} = \dfrac{3,36}{22,4} = 0,15(2)\\ \text{Phần 2 : Cu không phản ứng với axit loãng}\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(3)\\ (1)(2)(3) \Rightarrow a = b = 0,1 ; c = 0,15\)
Suy ra :
\(m_{Al} = 0,1.2.27 = 5,4(gam)\\ m_{Fe} = 0,1.2.56 = 11,2(gam)\\ m_{Cu} = 0,15.64.2 = 19,2(gam)\)
Đúng 1
Bình luận (0)
Đốt m gam hỗn hợp X gồm Fe, Cu, Mg, Zn trong oxi thu được 29,7 gam hỗn hợp chất rắn Y. Hòa tan hết Y bằng dung dịch HNO3 đặc nóng dư thu được 17,92 lit khí NO2 (đktc). Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được dung dịch Z chứa 84,1 gam muối và khí SO2. Biết rằng NO2 và SO2 là các sản phẩm khử duy nhất của HNO3 và H2SO4. Giá trị của m là A. 23,3 B. 20,1 C. 26,5 D. 20,9
Đọc tiếp
Đốt m gam hỗn hợp X gồm Fe, Cu, Mg, Zn trong oxi thu được 29,7 gam hỗn hợp chất rắn Y. Hòa tan hết Y bằng dung dịch HNO3 đặc nóng dư thu được 17,92 lit khí NO2 (đktc). Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được dung dịch Z chứa 84,1 gam muối và khí SO2. Biết rằng NO2 và SO2 là các sản phẩm khử duy nhất của HNO3 và H2SO4. Giá trị của m là
A. 23,3
B. 20,1
C. 26,5
D. 20,9
Đốt m gam hỗn hợp X gồm Fe, Cu, Mg, Zn trong oxi thu được 29,7 gam hỗn hợp chất rắn Y. Hòa tan hết Y bằng dung dịch HNO3 đặc nóng dư thu được 17,92 lit khí NO2 (đktc). Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được dung dịch Z chứa 84,1 gam muối và khí SO2. Biết rằng NO2 và SO2 là cac sản phẩm khử duy nhất của HNO3 và H2SO4. Gia trị của m là A. 23,3 B. 20,1 C. 26,5 D. 20,9
Đọc tiếp
Đốt m gam hỗn hợp X gồm Fe, Cu, Mg, Zn trong oxi thu được 29,7 gam hỗn hợp chất rắn Y. Hòa tan hết Y bằng dung dịch HNO3 đặc nóng dư thu được 17,92 lit khí NO2 (đktc). Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc, nóng, dư thu được dung dịch Z chứa 84,1 gam muối và khí SO2. Biết rằng NO2 và SO2 là cac sản phẩm khử duy nhất của HNO3 và H2SO4. Gia trị của m là
A. 23,3
B. 20,1
C. 26,5
D. 20,9
Ta có số mol e kim loại nhường là (19,7 - m)/8 + 0,8
Ta có số mol e nhận tạo khi SO2 là (19,7 -m)/8 + 0,8 => Số mol SO2 là (29,7 - m)/16 + 0,4
Trong phản ӭng với H2SO4 đặc, ta có số mol H2SO4 = số mol H2O = 2 số mol SO2
Áp dụng bảo toàn khối lượng => m = 26,5
=> Đap an C
Đúng 0
Bình luận (0)
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là A. 57,83%. B. 33,33%. C. 19,28%. D. 38,55%.
Đọc tiếp
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 57,83%.
B. 33,33%.
C. 19,28%.
D. 38,55%.
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n Cu = n SO 2 = 0 , 075 mol.
Đặt n Cr = x mol; n Fe = y mol → m X 52x + 56y + 0,075 × 64 = 18,2 gam.
x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
mCr trong X = 42,86% và %mCu trong X = 26,37%
Đáp án A
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Chọn đáp án A
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n C u = n S O 2 = 0 , 075 m o l
Đặt nCr = x mol; nFe = y mol ⇒ m X = 52x + 56y + 0,075 × 64 = 18,2 gam.
nH2 = x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
⇒ % mCr trong X = 42,86% và %mCu trong X = 26,37%
Đúng 0
Bình luận (0)